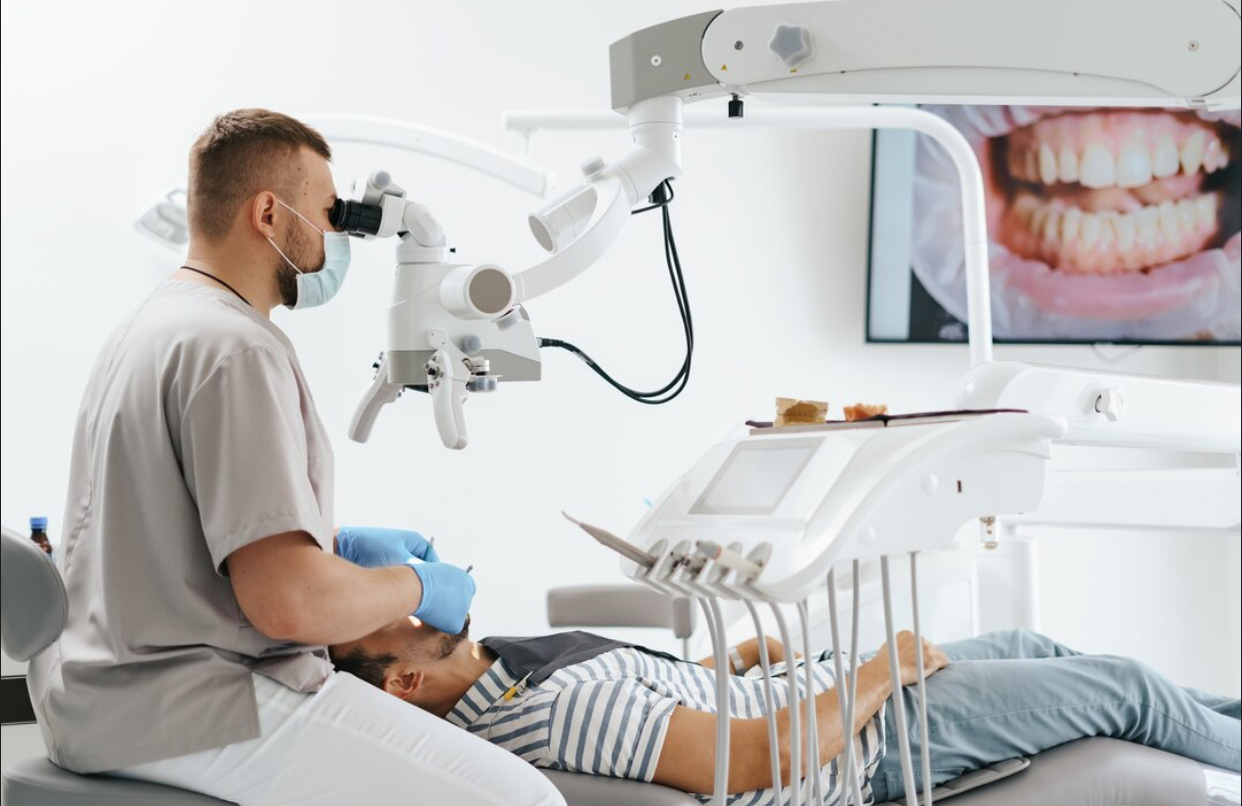
Noi măsuri pentru siguranța pacienților români. Crește calitatea tratamentelor
- Sabina Popescu
- 9 iunie 2021, 18:46

Guvernul a adoptat, miercuri, o nouă ordonanță de urgență prin care se stabilesc noi reglementări în vederea tratării pacientului.
Ministerul Sănătății a aprobat, miercuri, 9 iunie, desemnarea Agenției Naționale a Medicamentului şi a Dispozitivelor Medicale ca autoritate competentă în domeniul dispozitivelor medicale. De asemenea, Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale a fost numită și autoritate supremă în ceea ce privește supravegherea fluxului de dispozitive medicale din România.
Guvernul a adoptat o serie de măsuri privind dispozitivele medicale, specifice țărilor europene, și în statul român, pentru a asigura o bună funcționare a dispozitivele medicale astfel încât pacienții să aibă garanția unei tratări profesioniste.
Ce măsuri noi se adoptă
Executivul a aprobat, pe 9 iunie, o ordonanță de urgență prin care se are în vedere transparentizarea fluxului și a dispozitivelor medicale în sine. Cu alte cuvinte, dispozitivele medicale utilizate spre tratarea pacienților vor fi supuse unui sistem de calificare a tratamentelor, care permite verificarea istoricului dispozitivelor medicale, a utilizării sau a localizării lor prin identificări înregistrate.
La momentul utilizării unui dispozitiv medical, a unui tratament care are în vedere îmbunătățirea stării de sănătate a pacientului, prin noua ordonanță de urgență se impune prezentarea unui set de instrucțiuni de utilizare a dispozitivului în limba română.
"Se clarifică aspectul referitor la limba în care trebuie redactate informaţiile furnizate ca parte a unui sistem software, interfaţa echipamentelor de uz profesional cu utilizatorul", se arată într-un comunicat emis de către Ministerul Sănătății.
Promovarea dispozitivelor medicale poate fi sancționată
Conform informațiilor transmise de către Ministerul Sănătății, noi sancțiuni vor fi aplicate pentru cei care promovează și fac publicitate la diverse dispozitive medicale. "S-au stabilit contravenţii şi sancţiuni care vor fi aplicabile în situaţia nerespectării dispoziţiilor Regulamentului european", se arată în comunicat.
"Ordonanţa, care a fost adoptată la solicitarea Ministerului Sănătăţii, stabileşte cadrul instituţional, precum şi măsurile necesare pentru asigurarea aplicării directe a prevederilor Regulamentului (UE) 2017/745 al Parlamentului European şi al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 şi a Regulamentului (CE) nr. 1223/2009 şi de abrogare a Directivelor 90/385/CEE şi 93/42/CEE ale Consiliului.
Regulamentul (UE) 2017/745 armonizează normele pentru introducere pe piaţă şi punere în funcţiune a dispozitivelor medicale şi a accesoriilor pentru acestea pe piaţa Uniunii Europene, permiţându-le astfel să beneficieze de principiul liberei circulaţii a mărfurilor", mai transmite Ministerul Sănătății.