Vaccinul Pfizer, în cărți pentru aprobarea în regim de urgență! Când putem spera la prima doză în România
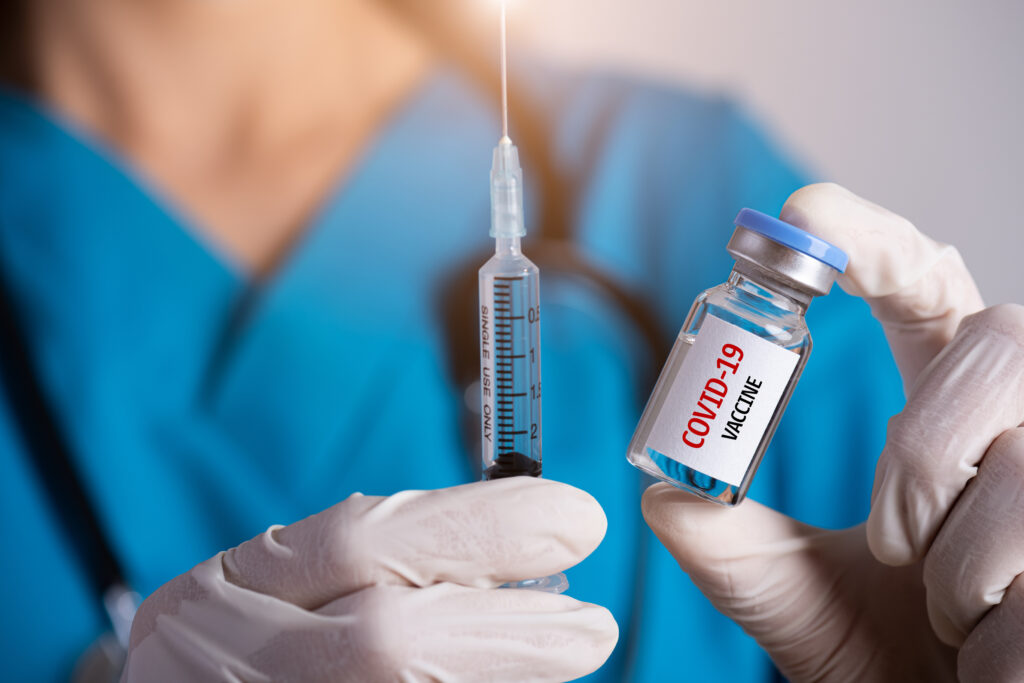
Compania americană Pfizer a anunțat, vineri, că ar putea aplica pentru aprobarea în regim de urgență a versiunii sale de vaccin Covid-19. Și celelalte companii concurente accelerează demersurile pentru aprobarea și punerea în circulație a vaccinurilor proprii.
Pfizer va aplica pentru aprobarea în regim de urgență a vaccinului său, la autoritatea care reglementează regimul medicamentelor în SUA, FDA, pentru versiunea pe care o dezvoltă alături de compania germană BioNTech, de îndată ce va trece ultimele teste de siguranță, estimate pentru a treia săptămână din noiembrie, a declarat președintele companiei, Albert Bourla, informează Reuters.
Potrivit oficialilor companiei, ultima fază și ultima a testărilor clinice se va încheia luna aceasta. FDA a anunțat că este nevoie de cel puțin o perioadă de două luni în verificarea siguranței produsului farmaceutic pentru a valida aprobarea în regim de urgență a oricărui vaccin experimental Covid-19. Totuși, este bună această precauție a procesului de aprobare, atrage atenția presa de peste Ocean, care menționează că FDA (Food and Drug Administration) a înăsprit reglementările de aprobare. Sondajele de opinie efectuate arată că majoritatea americanilor sunt foarte preocupați de siguranța unui vaccin Covid-19 și nu se vor grăbi să se vaccineze până când nu au certitudinea că vaccinul respectiv este viabil din punct de vedere al siguranței.
Cum stă concurența
Regeneron este o altă companie care a solicitat aprobarea în regim de urgență pentru vaccinul său, după ce președintele Trump a lăudat cocktailul de anticorpi al companiei pentru succesul terapiei sale de coronavirus. Regeneron spune că la început accesul la vaccinul său va fi extrem de limitat, cu doze doar pentru 50.000 de pacienți.
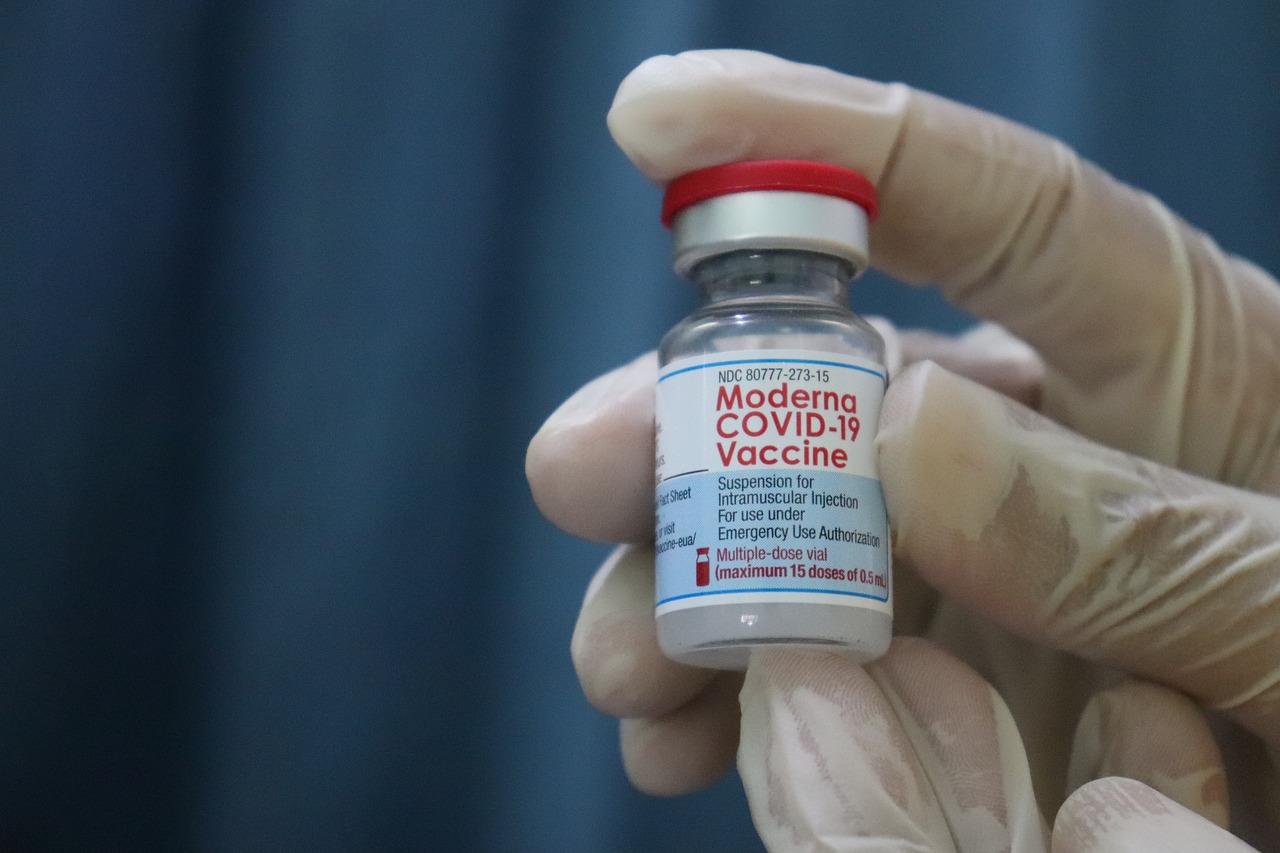
Joi, compania Moderna a anunțat că a primit confirmare scrisă de la Agenția Europeană pentru Medicamente că vaccinul său ar putea primi autorizare pentru piața din Uniunea Europeană. De vineri, 9 octombrie, studiul clinic pentru faza 3 a înregistrat aproape 30.000 de participanți.
Tot săptămâna aceasta, două tratamente cu anticorpi au cerut aprobarea în regim de urgență în SUA. Somități medicale americane spun că va mai dura însă un an sau doi până când astfel de medicamente vor rezolva problema coronavirusului.
Marți, studiul clinic de fază avansată în care este testat vaccinul dezvoltat de grupul american Johnson & Johnson a fost suspendat după ce un participant s-a îmbolnăvit. De asemenea, studiile clinice în care erau testate vaccinurile AstraZeneca /Universitatea Oxford au fost oprite temporar în lună cu o lună, după apariția unor reacții adverse severe la un participant. Ulterior, studiile clinice au fost reluate în Europa, după o decizie a autorităților de reglementare britanice, însă au rămas suspendate în SUA.
Primul studiu clinic pe copii
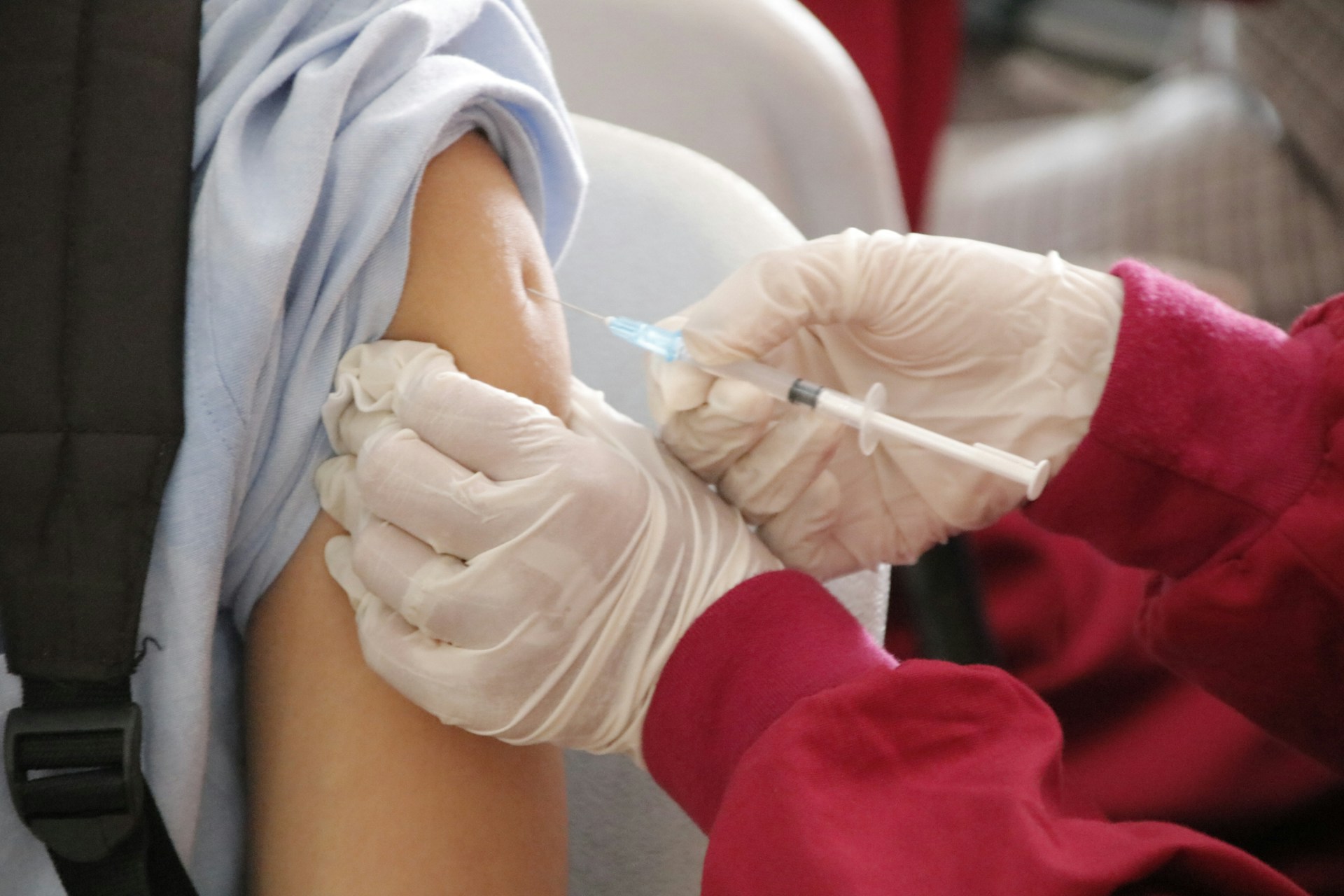
Joi, compania Pfizer a precizat că plănuiește să înceapă testarea vaccinului contra Covid-19 pe copii cu vârste începând de la 12 ani, iar părinții și-au exprimat deja dorința să își înscrie copiii. Astfel, va fi primul studiu clinic pentru un vaccin contra Covid-19 din Statele Unite care va include copii. Testarea va începe săptămâna viitoare pe copii cu vârste între 16 și 17 ani, iar ulterior se va trece la grupa de vârstă 12-15 ani, a declarat dr. Robert Frenck, directorul Centrului de Cercetare a Vaccinurilor din spitalul de copii din Cincinnati.