Tratament pentru întârzierea debutului diabetului de tip 1, propus pentru autorizare în Uniunea Europeană
- Andreea Răzmeriță
- 15 noiembrie 2025, 17:21
 Sursa foto: Freepik
Sursa foto: Freepik
Un tratament inovator, bazat pe un anticorp monoclonal, a demonstrat că poate întârzia apariția simptomelor diabetului de tip 1 la persoanele aflate în stadii incipiente ale bolii. Agenţia Europeană a Medicamentului (EMA) a recomandat autorizarea acestuia, oferind o nouă speranță în gestionarea unei afecțiuni care debutează frecvent la copii și necesită insulină zilnică încă de la primele simptome.
Diabetul de tip 1 și provocările tratamentului
Diabetul zaharat de tip 1 este o boală autoimună cronică în care sistemul imunitar distruge celulele beta din pancreas, responsabile de producerea insulinei. Lipsa acestui hormon împiedică utilizarea glucozei de către celule, ceea ce duce la simptome precum sete excesivă, foame, urinări frecvente, scădere în greutate și oboseală.
Boala evoluează în trei stadii, iar simptomele apar de obicei în stadiul 3, când pacienții au nevoie zilnic de insulină. În prezent, nu există tratamente autorizate care să întârzie sau să oprească debutul diabetului de tip 1, iar întârzierea instalării stadiului simptomatic poate reduce semnificativ povara terapiei, mai ales la copii.
EMA recomandă autorizarea unui nou tratament pentru diabetul de tip 1
Agenţia Europeană a Medicamentului (EMA) a recomandat autorizarea în Uniunea Europeană a tratamentului Teizeild (teplizumab) pentru întârzierea trecerii la stadiul 3 al diabetului zaharat de tip 1 la adulţi şi copii, începând de la vârsta de 8 ani cu boală în stadiul 2.
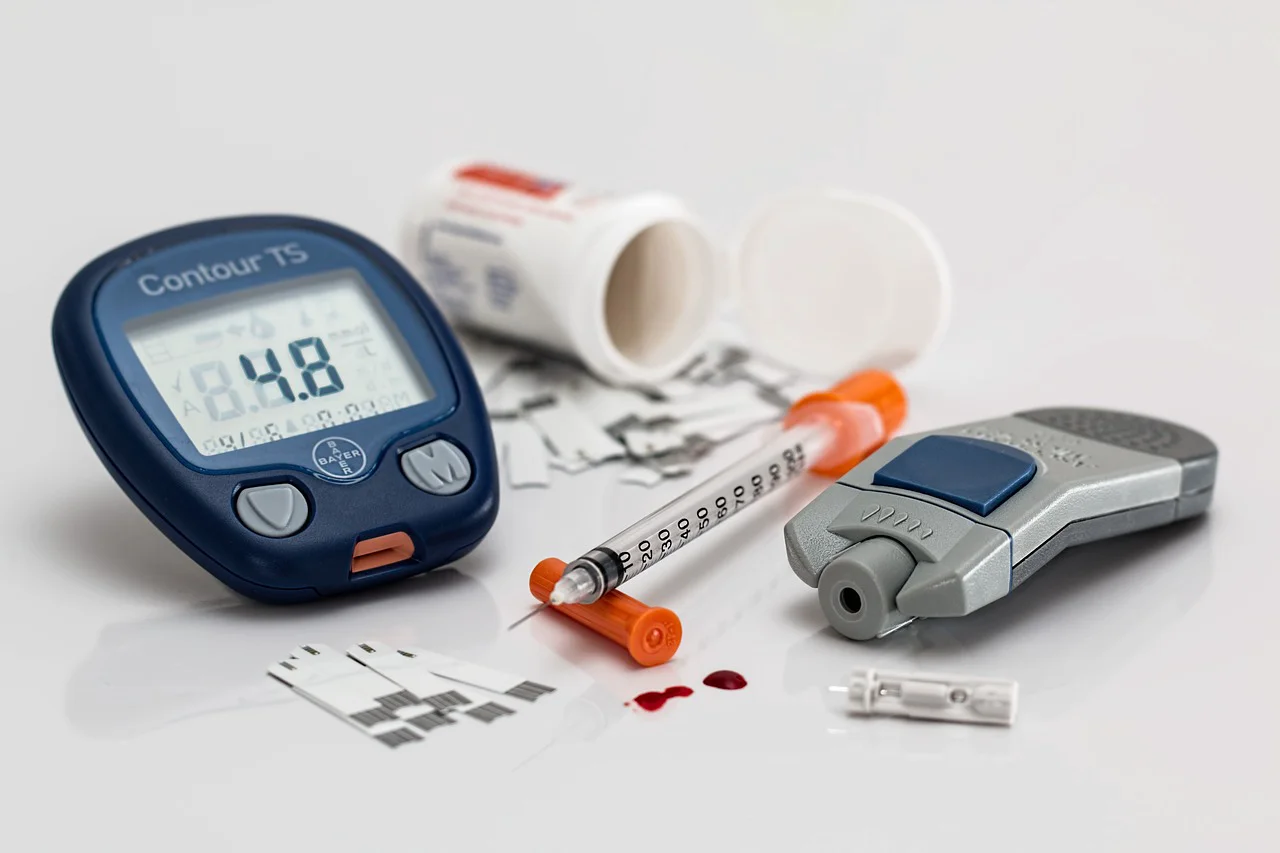
Diabet. Sursa foto Pixabay
Teplizumab este un anticorp care încetineşte progresia bolii prin reducerea ritmului de distrugere a celulelor beta. Administrarea se face intravenos, o dată pe zi, timp de 14 zile consecutive, iar dezvoltarea medicamentului a beneficiat de sprijin prin programul PRIME al EMA.
Rezultatele studiilor susţin recomandarea EMA pentru teplizumab
Recomandarea EMA se bazează pe un studiu clinic randomizat, dublu-orb, controlat cu placebo, realizat pe 76 de pacienţi cu diabet de tip 1 în stadiul 2. Pacienţii trataţi cu teplizumab au avut un timp mediu până la dezvoltarea stadiului 3 de 50 de luni, faţă de 25 de luni în grupul placebo.
Cele mai frecvente reacţii adverse au fost scăderea numărului unor tipuri de globule albe, erupţii cutanate şi valori reduse ale bicarbonatului sanguin. Sindromul de eliberare de citokine a fost raportat la 2% dintre pacienţi, iar planul de gestionare a riscurilor include monitorizarea şi reducerea acestor efecte.
Comisia Europeană va lua decizia finala privind aprobarea la nivelul Uniunii Europene.











