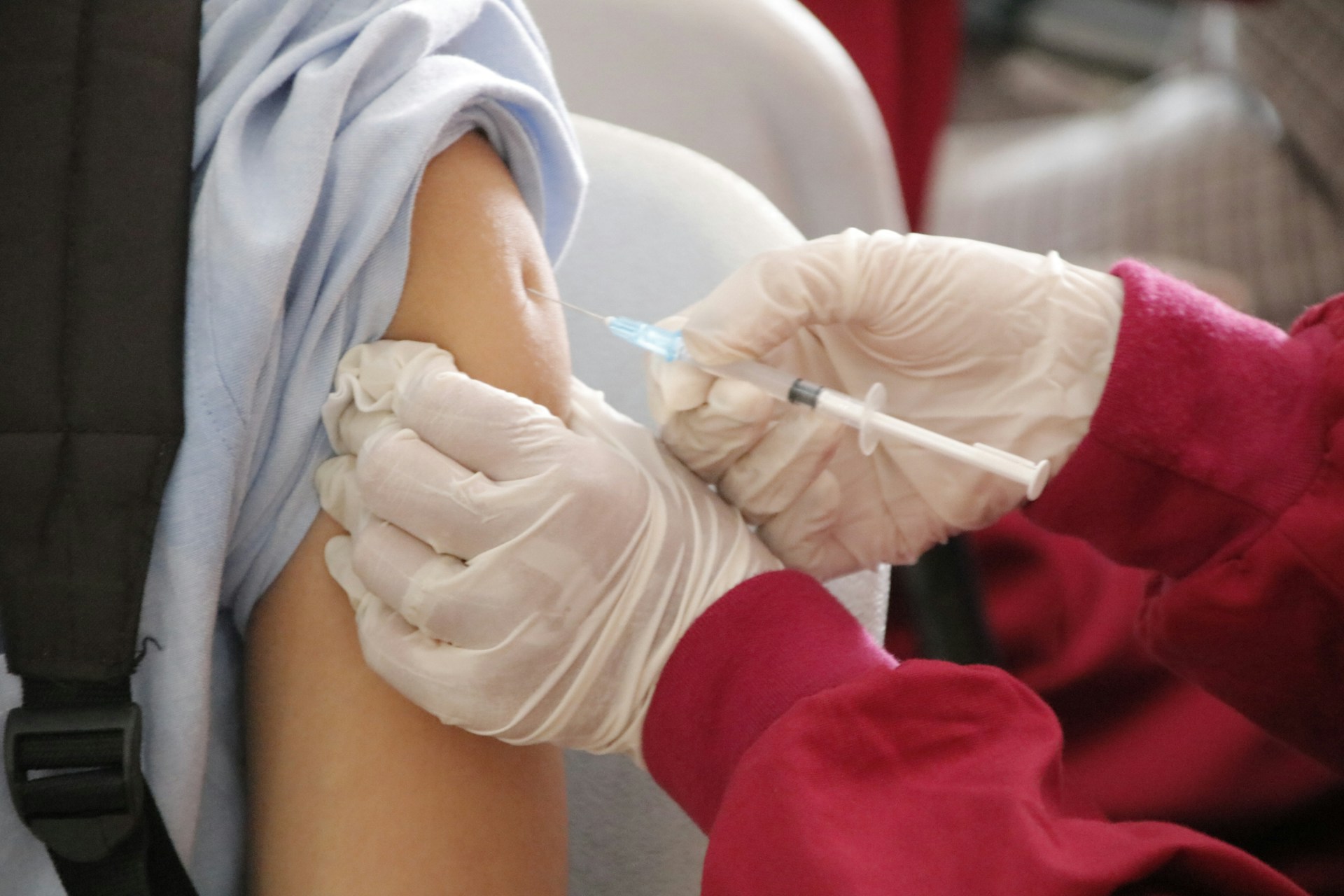
COVID-19. Bamlanivimab, aprobat în SUA! Speranță pentru sute de milioane de oameni
- Iuliu Vlădescu
- 10 februarie 2021, 10:54

- Bamlanivimab, aprobat în SUA! Decizia luată de FDA
- COVID-19. Medicament promițător: 29 din 30 de pacienți pleacă acasă după 5 zile
- Bamlanivimab și Etesevimab, administrate împreună
- Alertă mondială. Vaccin anti-coronavirus cu o sigură doză. Janssen Biotech (J&J) intră în lupta cu COVID-19
- Bamlanivimab, aprobat în SUA pentru a preveni decesele și cazurile grave
Bamlanivimab, aprobat în SUA! Medicamentul care folosește anticorpi monoclonali a primit autorizație de urgență din partea administrației americane pentru hrană și medicamente (FDA).
Bamlanivimab, aprobat în SUA! Deocamdată, FDA (Food and Drug Administration) a emis autorizarea de urgență pentru tratamentul combinat cu Bamlanivimab și Etesavimab pentru cazurile moderate de COVID-19. Medicamentul poate fi folosit în cazul adulților și copiilor de peste 12 ani (peste 40 de kilograme).
Această autorizare survine aprobării, tot de către FDA, a folosirii Bamlanivimab la adulți și copii cu risc de a devolta forme severe ale bolii COVID-19.
Autorizarea pentru aceste produse pe bază de anticorpi monoclonali le recomandă pentru pacienții testați pozitiv cu SARS-CoV-2 și care prezintă un risc ridicat de a dezvolta forme grave de COVID-19. Produsul poate fi folosit inclusiv peste persoanele de peste 65 de ani, cu comorbidități.
Bamlanivimab, aprobat în SUA! Decizia luată de FDA
Autorizarea a fost dată companiei Eli Lilly. Aprobarea s-a bazat pe dovezile dintr-un studiu clinic. Acesta a arătat că o singură administrare intravenoasă de Bamlanivimab și Etesevimab reduce semnificativ durata de spitalizare și riscul de deces legate de infecția cu coronavirus.
Studiul, randomizat, dublu-orb și controlat prin administrarea de placebo a inclus 1.035 de adulți nespitalizați cu forme ușoare sau medii de COVID-19, dar cu risc de a dezvolta forme severe.
COVID-19. Medicament promițător: 29 din 30 de pacienți pleacă acasă după 5 zile
Cercetătorii a administrat o singură injecție cu Bamlanivimab de 2800 mg și Etesevimab de 2800 mg la 518 pacienți, și placebo la 517 pacienți.
Bamlanivimab și Etesevimab, administrate împreună
Dintre pacienții ce au primit placebo s-au înregistrat 36 (7%) de spitalizări și decese, față de doar 11 (2%) la pacineții ce primiseră combinația celor doi anticorpi monoclonali. Aceasta reprezintă o scădere a riscului de deces cu 70% la 29 de zile.
Mai mult, toate cele 10 decese au survenit la pacienții ce primiseră placebo.
Alertă mondială. Vaccin anti-coronavirus cu o sigură doză. Janssen Biotech (J&J) intră în lupta cu COVID-19
Investigatorii FDA continuă să studieze siguranța și eficacitatea acestei terapii pentru COVID-19.
Anterior, Bamlanivimab primise aprobarea FDA ca terapie singulară (cu o doză de 700 mg) pentru cazurile ușoare și medii de COVID-19. Aprobarea era tot pentru populația de la 12 ani în sus.
Bamlanivimab, aprobat în SUA pentru a preveni decesele și cazurile grave
Acum, aprobarea acestei terapii ce combină anticorpi se face în încercarea de a elimina cât mai mult din riscul de deces sau de forme grave în urma infecției cu coronavirus.
“The data supporting this emergency authorization add to emerging evidence that points to the clinical utility of neutralizing antibodies for the treatment of COVID-19 in certain patients,” Patrizia Cavazzoni, MD, acting director of
„Ca parte a programului nostru de accelerare a tratamentuluipentru coronavirus, FDA folosește orice resursă are la dispoziție. Este și cazul acestei terapii cu anticorpi monoclonali, care rămâne în studiu”, a declarat medicul Patrizia Cavazzoni, director al FDA, citată de ContagionLive.